2 ECUACIÓN DE EQUILIBRIO DE
EXCITACIÓN DE BOLTZMANN
Si un determinado sistema físico se encuentra en
condiciones de equilibrio termodinámico estricto, la Física Clásica predice
entonces que la probabilidad P(E) de
que una partícula de dicho sistema tenga una cierta energía E, es proporcional al denominado factor de Boltzmann e-E/kT.
Una simple gráfica de P(E) en función
de la energía E demuestra que el
factor de Boltzmann tiende a favorecer los estados de baja energía (Figura 4-1). Por otra parte, dado que el
factor de Boltzmann aumenta con la temperatura, la población de un determinado
nivel E aumentará también a medida
que se incrementa la temperatura, siempre que se trate de niveles elevados.
El punto de vista anterior está de acuerdo con la Física
Clásica. En los sistemas mecánico-cuánticos también existe la misma dependencia
con la energía, sólo que en este caso hay que tener en cuenta la degeneración del nivel. En efecto,
recordemos que la descripción mecánico-cuántica completa del estado de
excitación de un átomo, requiere el conocimiento de cuatro números cuánticos.
En general, suele interesar la energía del átomo y no su estado
mecánico-cuántico completo. Sin embargo, pueden existir varios estados
mecánico-cuánticos diferentes correspondientes a un único valor de la energía.
El número de tales estados que
corresponde a un cierto nivel de energía se denomina el peso estadístico o degeneración
del nivel. En términos de la Mecánica Cuántica, la anterior aseveración se
expresa diciendo que pueden existir diferentes funciones de onda (autovectores)
que corresponden a un mismo autovalor de la energía. La degeneración del nivel se pone en evidencia ante la presencia de un
campo magnético, pues éste desdobla el nivel en diferentes estados Zeeman. El
peso estadístico del nivel resulta ser 2J+1,
donde J es el número cuántico
correspondiente al momento angular total de átomo. El peso estadístico del
nivel es 2J+1, ya sea que existan
condiciones de acoplamiento LS o j-j.
Resulta evidente que la probabilidad de que un
nivel con alto peso estadístico sea ocupado, es mayor que la probabilidad de
que esto ocurra en un nivel con bajo peso estadístico. La expresión clásica
(factor de Boltzmann) debe ser entonces modificada; la probabilidad de que un
átomo tenga una energía E debe ser
ahora proporcional al producto g(E). e-E/kT,
siendo g(E) el peso estadístico del
nivel de energía E.
Sean Nj y Nk los
números de átomos, por unidad de volumen, con energías Ej y Ek
respectivamente. La población relativa de los dos niveles, por unidad de
volumen, será :
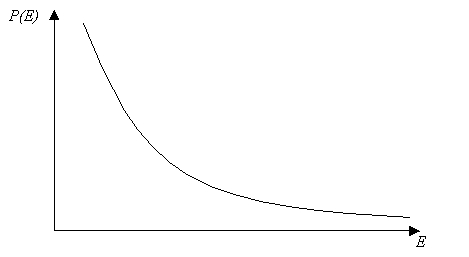
Figura 4-1. La probabilidad de que una
partícula tenga un cierta energía E de acuerdo a la Física Clásica varía
exponencialmente con la energía
![]() (4.1)
(4.1)
Enverdad, la ecuación (4.1) es correcta cuando
los valoresErepresentan las energías
totales que posee el átomo. Sin embargo,dicha ecuación puede ser aplicada
separadamente a cada clase de energía quetiene el átomo. En nuestro casoErepresentará sólo las energías de
excitación y ionización.
Supongamos ahora queNijrepresenta el número de
átomos por unidad de volumen en el estado de ionizacióniy en el nivel de excitaciónj.
El nivel fundamental de cualquierestado de ionización es j= 1 y los niveles excitados tienenvalores enteros dejdesde 2 hastainfinito.
Sabemos que el electrón que alcanza lavelocidad
de escape define el punto cero de energía. Por definición, diremosahora que el
cero de la energía corresponde al nivel fundamental del estado deionización de
interés. Con esta nueva definición, los niveles excitados tendránenergías
positivas. Debe notarse que la ecuación (4.1) incluye sólo lasdiferencias de
los niveles de energía y no los valores absolutos de los mismos.Por lo tanto,
dichas diferencias no alteran si a cada nivel se le agrega unamisma constante.
Escribiremos entonces la expresión (4.1) de la siguientemanera :
![]() (4.2)
(4.2)
O bien :
![]() (4.3)
(4.3)
en la cualE1j = (Ej– E1)representa el exceso de energía del
niveljsobre el nivel fundamental.
Dicho exceso se conoce comopotencial de
excitacióndel nivelj. La ecuación
(4.3) constituye una de las formas más conocidas delaecuación de equilibrio de excitaciónde Boltzmann.
SiNirepresenta el número total de átomos en el estado de
ionizacióni, por unidad de volumen,
entonces :
![]() (4.4)
(4.4)
DespejandoNijde (4.3) y sumando sobre el índicej,tenemos :
![]()
![]()
![]() (4.5)
(4.5)
La sumatoria anterior se denominafunción
de particióndel estado de
ionizacióniy usualmente se denotaUi, es decir :
![]()
![]() (4.6)
(4.6)
Dichafunción es la suma, sobre todos los niveles
ligados, de los productos de lospesos estadísticos por los factores de
Boltzmann. En muchos casos, lascondiciones son tales que casi todos los átomos
están en el nivel fundamental. Entales casos, domina el primer término en (4.6)
y la función de particiónresulta aproximadamente igual al peso estadístico del
nivel fundamental.
Elcociente entre las expresiones (4.3) y (4.5)
da lugar a otra forma bienconocida de laecuación de Boltzmann:
![]() (4.7)
(4.7)
Tomando logaritmos en la expresión
anterior y teniendo en cuenta quela constante de Boltzmannkvale1.38x10-16ergios
°K-1y que un electrón-volt es equivalente a 1.603x10-12ergios, resulta :
![]() (4.8)
(4.8)
o bien :
![]() (4.9)
(4.9)
en la cualTse
expresa en grados Kelvin yEijeneV.
Para el átomo de hidrógeno (j=n),
el peso estadístico del nivelnes 2n2y los potenciales de
excitación pueden obtenerse apartir de (3-17), conZ=1. Sinembargo, teniendo en cuenta el nuevo punto cero de la
energía adoptado, debemosagregar 13.6eVa
los valores dadosen (3-17). Así resulta:
![]() (4.10)
(4.10)
Si se supone que aproximadamente
todo elHneutro está en el nivel
fundamental, entoncesU1= 2
y de (4.9) resulta :
![]() (4.11)
(4.11)
En laTabla (4.1)semuestran algunos valores numéricos deN1n/N1calculados de laexpresión (4.11). Es evidente que a
medida que aumenta la temperatura, seincrementa también la población de los
niveles más altos. Se aprecia además quepara bajas temperaturas, la
aproximación de que todo el hidrógeno neutro estáen el nivel fundamental, es
más que razonable.
TABLA 4–1
T =5000°K
T= 15000°K T= 25000°K
n= 2 2.1x10-10 1.5x10-3 3.5x10-2
n= 3 5.9x10-12 7.8x10-4 3.3x10-2
n= 4 4.2x10-11 8.4x10-4 4.3x10-2