 Hans Bethe
Hans Bethe
 Hans Bethe
Hans Bethe
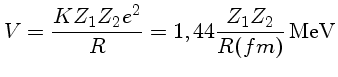
A energia cinética entre as partículas é determinada por uma distribuição de velocidades de Maxwell-Boltzmann correspondente à energia térmica
| Reaçăo | Tmínima |
|---|---|
| 41H—»4He | 8 milhőes K |
| 34He—»12C | 100 milhőes K |
| 212C—»24Mg | 1 bilhăo K |
Hans Bethe tomou os melhores dados das reações nucleares existentes e mostrou, em detalhe, como quatro prótons poderiam ser unidos e transformados em um núcleo de hélio, liberando a energia que Eddington havia sugerido. O processo que Bethe elaborou em seu artigo, conhecido atualmente como o Ciclo do Carbono, envolve uma cadeia complexa de seis reações nucleares em que átomos de carbono e nitrogênio agem como catalisadores para a fusão nuclear. Naquela época, os astrônomos calculavam que a temperatura no interior do Sol fosse de cerca de 19 milhões de graus Kelvin, e Bethe demonstrou que àquela temperatura, o ciclo do carbono seria o modo dominante de produção de energia.
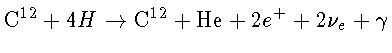

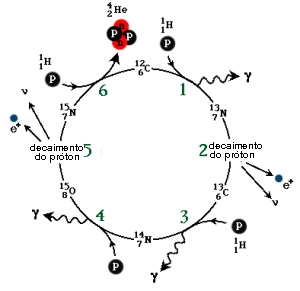

Na mesma época, além de Hans Bethe, o físico alemão Carl Friedrich von Weizäcker (1912-2007) e Charles Critchfield (1910-1994) identificaram várias das reações de fusão nuclear que mantém o brilho das estrelas. Hoje em dia, o valor aceito para a temperatura do núcleo do Sol é de 15 milhões de graus Kelvin, e à esta temperatura, como explicitado por Bethe no seu artigo, o ciclo próton-próton domina. O ciclo próton-próton necessita de T > 8 milhőes de K para ser efetivo.
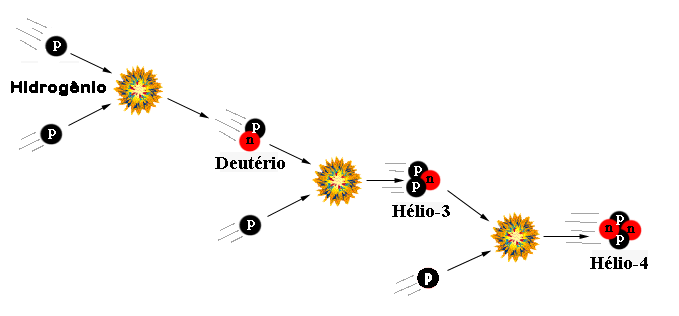
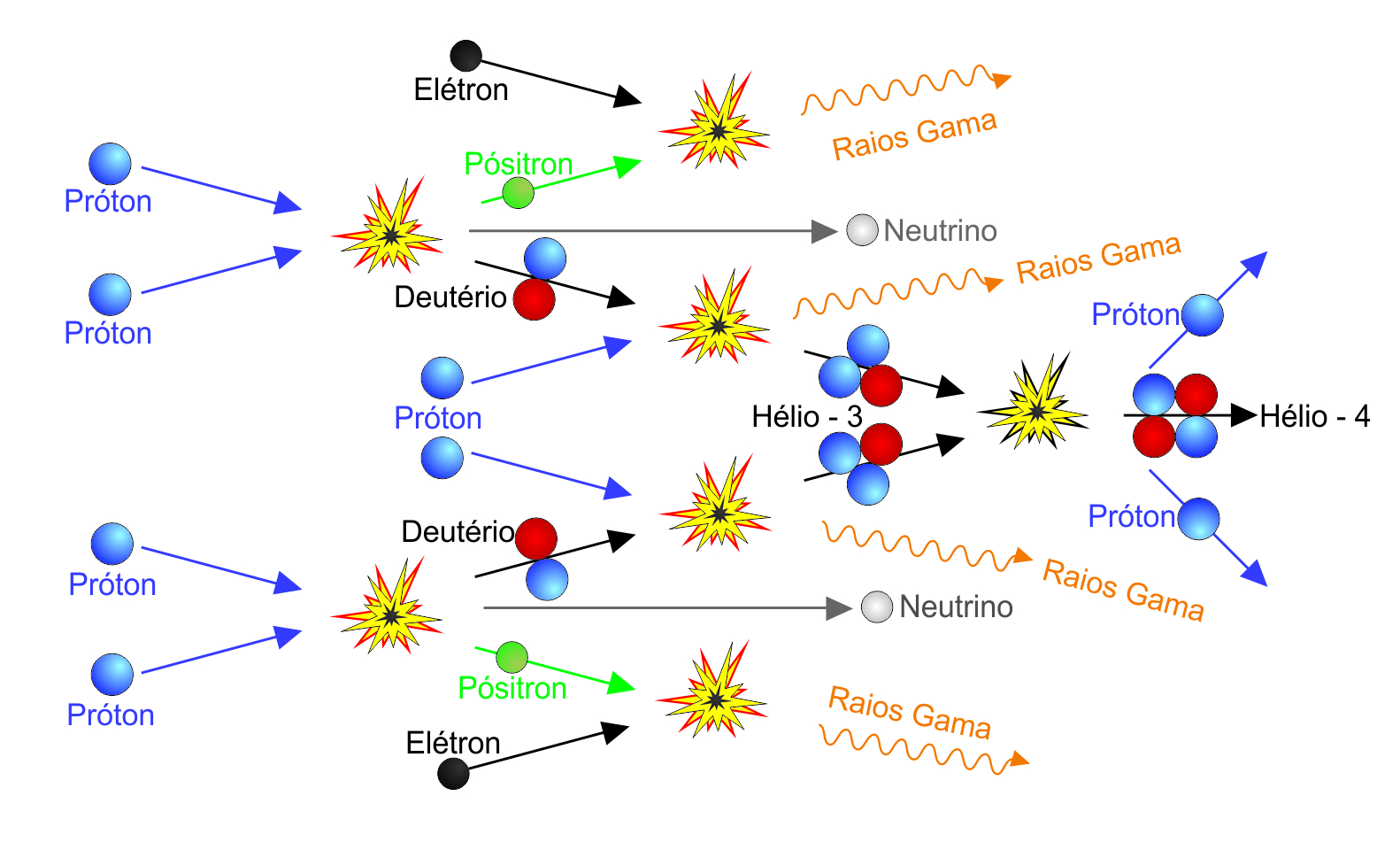
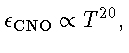
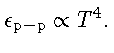
A astrofísica demonstrou que as leis físicas que conhecemos em nossa limitada experiência na Terra são suficientes para estudar completamente o interior das estrelas. Desde as descobertas de Bethe, o cálculo de evolução estelar através da união da estrutura estelar com as taxas de reações nucleares tornou-se um campo bem desenvolvido, e astrônomos calculam com confiança o fim de uma estrela como nosso Sol daqui a 6,5 bilhões de anos como uma anã branca, após a queima do hélio em carbono pela reação triplo-α:
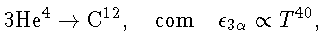
Para comparar, a primeira bomba atômica, de urânio, chamada de Little Boy e que explodiu sobre a cidade de Hiroshima, tinha uma potência de 20 000 toneladas de TNT (tri-nitro-tolueno, ou nitroglicerina). Uma bomba de hidrogênio tem uma potência de 20 milhões de toneladas de TNT.
| Química | Fissão | Fusão | |
|---|---|---|---|
| Exemplos de reação | C + O2 -> CO2 | n + U235 -> Ba143 + Kr91 + 2 n | H2 + H3 -> He4 + n |
| Combustível Típico | Carvão | UO2 (3% U235 + 97% U238) | Deutério & Lítio |
| Temperatura para reação (C) | 873 | 1273 | 1 000 000 |
| Energia liberada por kg de Combustível (J/kg) | 3,3 × 107 | 2,1 × 1012 | 3,4 × 1014 |
O conceito de entropia está intimamente ligado ao conceito de calor. Quando um sistema recebe entropia (calor), ele recebe energia. Se um corpo a uma temperatura T recebe entropia (S), ele absorve energia (E) equivalente ao produto da temperatura pela entropia.
Notas históricas: A descoberta da fissão nuclear ocorreu em 10 de dezembro de 1938 e foi descrita em um artigo submetido ao Naturwissenchaften em 22 de dezembro de 1938, pelos alemães Otto Hahan (1879-1968), Fritz Strassmann (1902-1980) e pela austríaca Lise Meitner (1878-1968).
O italiano Enrico Fermi (1901-1954) foi uma das pessoas mais importantes no desenvolvimento teórico e experimental da bomba atômica. Sua esposa, Laura Fermi, era judia. Quando Benito Mussolini (1883-1945) aprovou o Manifesto della Razza em 14 de julho de 1938, impondo leis racistas na Itália facista, Enrico decidiu aceitar o emprego oferecido pela Columbia University, nos Estados Unidos. Ele e sua família partiram de Roma para a cerimômia de entrega do Prêmio Nobel à Fermi em dezembro de 1938 e nunca retornaram à Itália. O Nobel foi lhe dado por seu estudo de radioatividade artificial, com suas experiências de bombardeamento de urânio com nêutrons, criando novos elementos mais pesados, e seu aumento pela redução da velocidade dos nêutrons. Fermi havia descoberto que quando ele colocava uma placa de parafina entre a fonte de nêutrons e o urânio, aumentava a radioatividade, pois aumentava a chance do nêutron ser absorvido pelo núcleo de urânio.
Em 1934 o húngaro Leo Szilard (1898-1964) já havia patenteado a idéia da reação em cadeia e em 2 de dezembro de 1942 Fermi conseguiu construir uma massa crítica de U235/U238 não separados (na natureza somente 0,7% são do U235 que é ativo), usando grafite para reduzir a velocidade dos nêutrons e acelerar a produção de nêutrons secundários. Na experiência ele utilizou barras de cádmium como absorsores de nêutrons para regular a experiência e produziu um crescimento exponencial do número de nêutrons, isto é, uma reação em cadeia.
Em 1939 os físicos já sabiam que água pesada agia como um moderador, isto é, redutor de velocidade dos nêutrons, como a parafina. A água normal (leve) consiste de dois átomos de hidrogênio e um átomo de oxigênio (H2O). Na água pesada, dois isótopos de hidrogênio, deutério, se unem com o oxigênio. Água pesada é ainda hoje utilizada como moderador em reatores nucleares de urânio natural.
Em 1939 Szilard convenceu Albert Einstein (1879-1955), com quem ele tinha trabalhado em 1919 em Berlin, a mandar uma carta para o presidente americano Franklin Delano Roosevelt (1933-1945) sobre o desenvolvimento pelos alemães de armas atômicas e pedindo ao presidente que iniciasse um programa americano, que mais tarde se chamaria Projeto Manhatam, chefiado pelo americano Julius Robert Oppenheimer (1904-1967) e levaria ao desenvolvimento do Los Alamos National Laboratory, ao teste Trinity, em 16 julho 1945, com a explosão da primeira bomba atômica em Alamogordo, New Mexico, e à construção das bombas Little Boy (20 ton T.N.T) e Fat Man, que seriam utilizadas em Hiroshima e Nagasaki em 6 e 9 de agosto de 1945.
O húngaro Edward Teller (1908-2003), sob protestos de Fermi e Szilard, chefiou o desenvolvimento da bomba de fusão de hidrogênio, que utiliza uma bomba de fissão como gatilho para iniciar a colisão do deutério com o trítio. A bomba de hidrogênio, Mike, de 10,4 Mton T.N.T. foi testada em 31 de outubro de 1952, em Eniwetok.
Quando 2 átomos de hidrogênio se transformam em deutério, no
primeiro passo da fusão do hidrogênio
|
| Processo Termonuclear |
Massa na Seqüęncia Principal Necessária para a Queima (MSol) |
Temperatura de Igniçăo (K) |
Densidade Aproximada (g/cm3) |
Elétrons Degenerados para Densitidades Maiores que (g/cm3) |
|---|---|---|---|---|
| Queima de Hidrogęnio 4H->He |
0,08 | 4 × 106 | 10-102 | ~103 |
| Queima de Hélio 3He->C, O |
0,4 | 120 x 106 | 103-106 | ~105 |
| Queima do Carbono 2C->Ne, Na, Mg, O |
8 | 600 × 106 | 105-108 | ~107 |
| Queima de Oxigęnio, Neônio e Silício Ne-->O,Mg O-->S,Si,P Si-->Ni-->Fe |
10,5 | 1 × 109 a 3 × 109 |
>107 | ~109 |
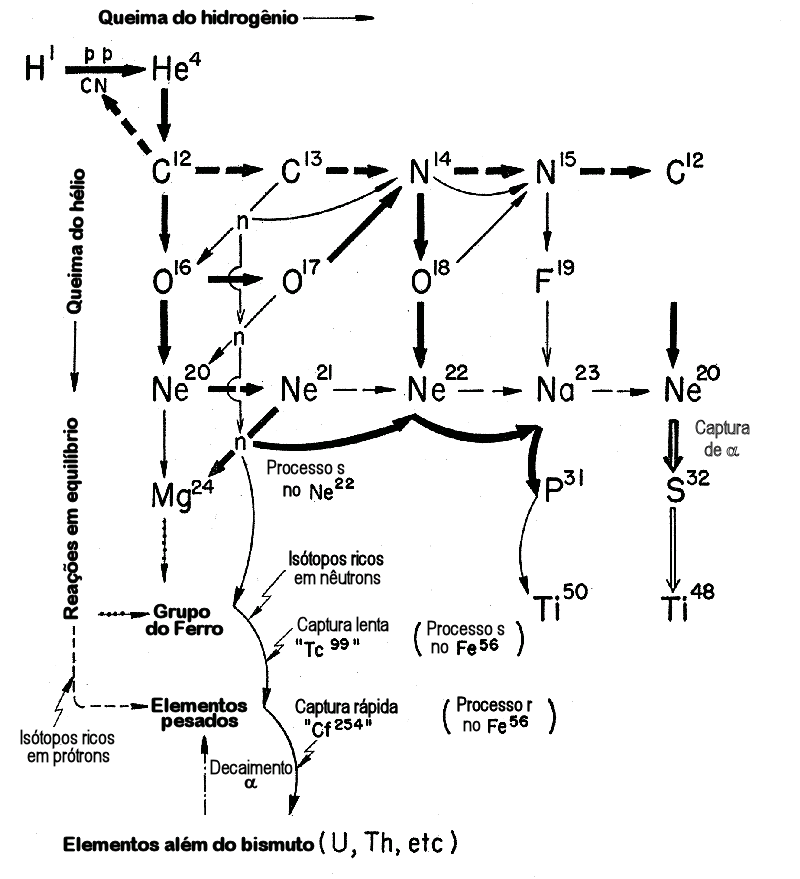
Mais detalhes em
http://www.atomicarchive.com/
http://www.time.com/time/time100/scientist/profile/fermi.html
http://www.dannen.com/szilard.html