A energia total necessária para separar um núcleo em seus prótons e nêutrons pode ser calculada a partir da energia nuclear de ligação. Para um núcleo com Z prótons e (A-Z) nęutrons, onde A é a massa atômica,

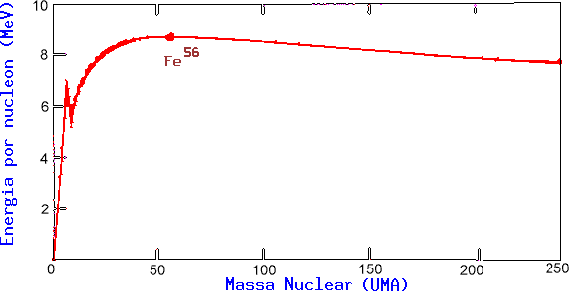
A queda da energia de ligação por núcleon para números de massas maiores que 56 indicam que estes núcleons são mais compactados formando dois nuclidios de massa intermediária, em vez de um único nuclidio de alta massa. Em outras palavras, energia pode ser liberada pela fissão nuclear do nuclidio de alta massa em dois nuclidios de massa intermediária. A fissão foi descoberta em 1938 por Otto Hahn (1879-1968), Fritz Strassmann (1902-1980) e Lise Meitner (1878-1968).
O aumento da energia de ligação para baixos valores de número de massa, ao contrário, nos indica que energia será liberada se dois nuclidios de baixa massa se combinarem, formando um único nuclidio de massa intermediária. Este processo é chamado de fusão nuclear. Uma bomba de hidrogênio, contruída pela primeira vez em 1952, funde deutério e trítio, formando hélio e liberando um nêutron e 17,6 MeV de energia.
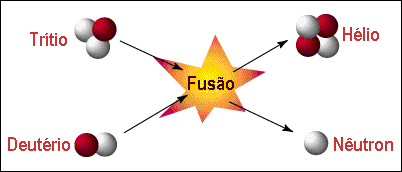
O radioisótopo trítio do hidrogênio, com massa 3,014 u.m.a, foi produzido em aceleradores em 1932 por Lord Rutherford [Ernest Rutherford (1871-1937)], Sir John Douglas Cockroft (1897-1967) e Ernest Orlando Lawrence (1901-1958), e foi caracterizado por Luis Walter Alvarez (1911-1988). Sua vida média é de 12,35 anos, decaindo por emissão de um elétron em He3 e liberando 18,6 KeV de energia. Na natureza ele é produzido pela colisão de raios-cósmicos com nêutrons do ar e trazido para a superfície da Terra pela chuva. Willard Frank Libby (1908-1980), o proponente do método de datação por carbono-14, usava o decaimento do trítio como método de datação da idade dos vinhos: um vinho de 20 anos deve conter somente um terço da quantidade de trítio observada em água de chuva fresca.
O método de datacão por carbono 14 (C14) foi desenvolvido logo após a segunda guerra mundial. O C14 é radiativo, é produzido pelo bombardeamento de nitrogênio 14 por raios cósmicos na atmosfera e é absorvido do ar pelas plantas. Animais comem as plantas e absorvem o C14. Humanos absorvem o C14 ao comerem plantas e animais. Quando um organismo morre, ele para de absorver C14 e a quantidade já existente no organismo começa a decair em N14, com uma vida média de 5730 anos. Para descobrir há quanto tempo um organismo morreu, determina-se a quantidade de elétrons emitidos por grama do material. Atualmente o C14 emite cerca de 15 elétrons por minuto por grama do material. Antes da explosão da primeira bomba atômica na biosfera da Terra, ocorriam aproximadamente 13,5 emissões de elétrons por minuto por grama do carbono. Se uma material emite 13,5/2 elétrons por minuto por grama, o organismo deve ter 5730 anos.